Dans une nouvelle étude, l’équipe de recherche du Pr Jonathan Weitzman au sein du laboratoire Épigénétique et Destin Cellulaire a mis en lumière le mécanisme par lequel le parasite Theileria annulata, responsable de maladies semblables aux cancers chez les bovins, échappe au mécanisme de défense de la cellule hôte. Dans une précédente étude, l’équipe avait montré comment Theileria annulata parvient à rendre cancéreuses les cellules qu’il infecte, en sécrétant une protéine qui active des voies génétiques et épigénétiques. Aujourd’hui, Marie Villares, (doctorante, première auteure de cette étude) et l’équipe de chercheurs, ont découvert et décryptent la façon dont Theileria annulata échappe au mécanisme de nettoyage et recyclage de la cellule, appelé autophagie.
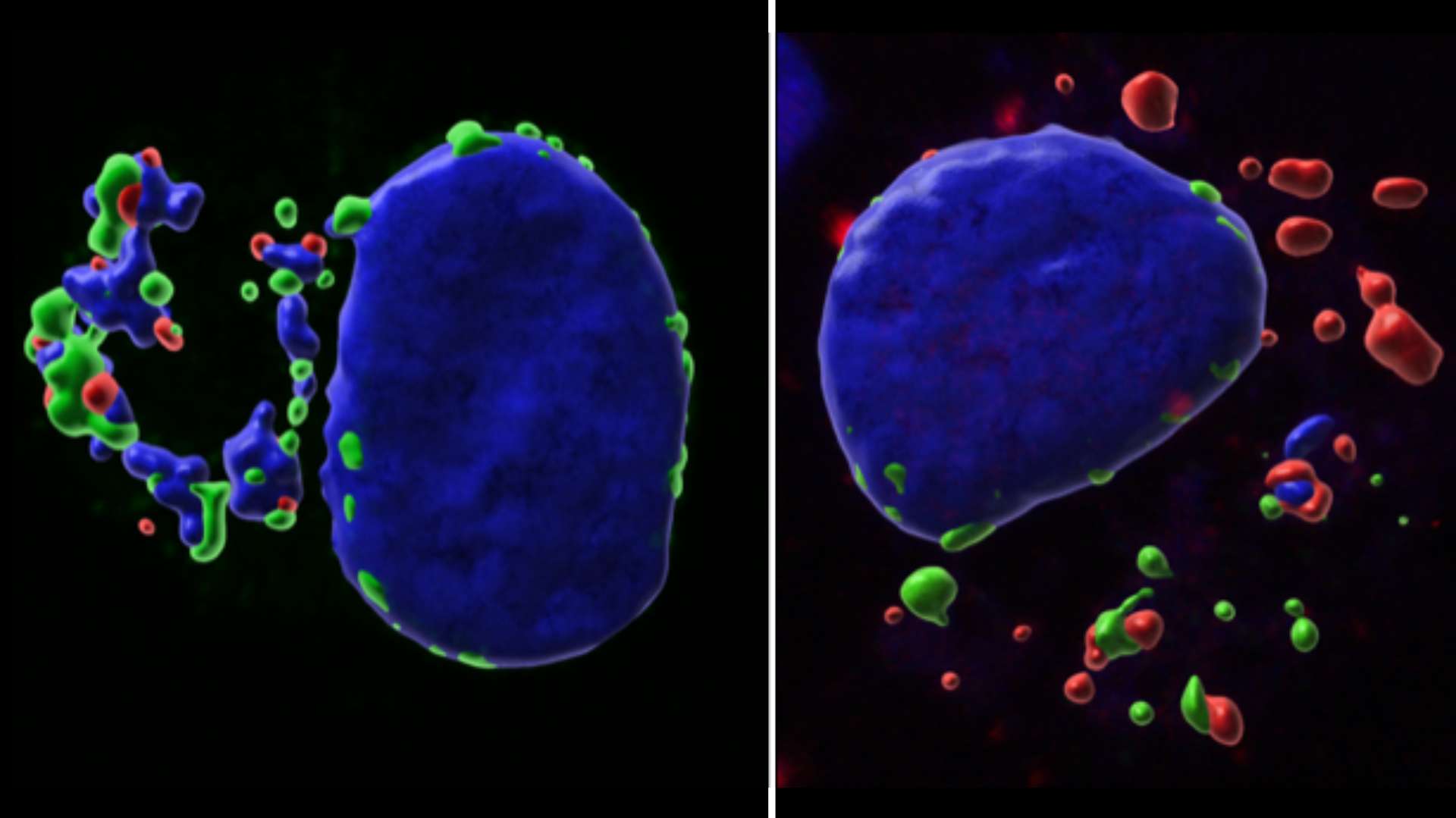
Images prises au microscope de cellules (en bleu) traitées ou non avec le composé étudié, montrant une différence de localisation des protéines d’intérêt (en vert et rouge) entre les deux conditions.
© Marie Villarès – Université Paris Cité
Toutes les cellules mammifères disposent d’un processus de nettoyage spécialisé appelé « autophagie » qui recycle les protéines endommagées et élimine les agents pathogènes envahissants. Pour survivre à l’intérieur des cellules hôtes, les agents pathogènes doivent trouver un moyen d’échapper à l’autophagie. Theileria annulata, parasite unicellulaire transmis à la vache par les tiques, provoque une maladie mortelle chez les bovins en Afrique et en Asie, avec un impact socio-économique très conséquent. Ce parasite se divise et multiplie au même rythme que les globules blancs qu’il infecte, et les rend, tout comme des cellules cancéreuses, « immortels ».
Dans une précédente étude, les généticiens et biochimistes, membres du laboratoire Épigénétique et Destin Cellulaire, avaient montré que le parasite Theileria annulata sécrète une protéine qui active certains gènes du globule blanc infecté, et le transforme en cellule cancéreuse. Ce mécanisme, encore jamais décrit chez les mammifères, ouvrait de nouvelles pistes thérapeutiques. Pour autant, le parasite n’avait pas livré tous ses secrets. Comment arrive-t-il à survivre dans les environnements hostiles des cellules hôtes et échapper au système immunitaire ?
Le parasite Theileria annulata, devrait être éliminé grâce au mécanisme d’autophagie de la cellule hôte. Il semble donc que ce mécanisme ne soit pas efficace contre ce parasite. En testant des centaines de molécules initialement créées pour leurs propriétés anti-cancéreuses, Marie Villares a identifié une molécule qui permet à la cellule hôte d’éliminer le parasite. Par différentes techniques de génomique, de protéomique, d’imagerie, elle a ensuite décrypté le mécanisme par lequel cette molécule agit dans la cellule infectée. En comprenant comment la molécule agit, Marie Villares et l’équipe de chercheurs ont aussi découvert comment le parasite Theileria annulata échappe à l’autophagie pour survivre dans la cellule hôte, le globule blanc infecté. Une fois entré dans la cellule qu’il infecte, le parasite séquestre, à sa surface, une protéine (eIF5A) de la cellule, essentielle au processus de nettoyage par autophagie. eIF5A étant inhibée, la cellule ne peut plus se défendre. La molécule capable de redonner son efficacité au processus d’autophagie agit en libérant eIF5A de l’emprise du parasite. Le processus d’autophagie peut alors reprendre son activité au sein de la cellule et éliminer le parasite.
Cette étude révèle un nouveau mécanisme utilisé par les parasites intracellulaires, comme Theileria annulata, pour échapper aux défenses de la cellule hôte par le processus d’autophagie. La molécule identifiée comme libératrice de eIF5A pourrait être un nouveau médicament utilisé pour traiter les vaches infectées et éliminer ce dangereux pathogène.
Ce travail est le fruit d’une collaboration internationale avec une équipe de chimistes médicinaux de l’Université Sapienza à Rome, en Italie, et des collègues des plateformes technologiques d’imagerie et de protéomique de l’Institut Jacques Monod. L’équipe du Pr Weitzman est soutenue par des subventions de l’ANR, du Labex Who Am I?, du Graduate School G.E.N.E. et de la Fondation pour la Recherche Médicale (Equipe FRM).
Référence
Theileria parasites sequester host eIF5A to escape elimination by host-mediated autophagy – Marie Villares, Nelly Lourenço, Ivan Ktorza, Jérémy Berthelet, Aristeidis Panagiotou, Aurélie Richard, Angélique Amo, Yulianna Koziy, Souhila Medjkane, Sergio Valente, Rossella Fioravanti, Catherine Pioche-Durieu, Laurent Lignière, Guillaume Chevreux, Antonello Mai & Jonathan B. Weitzman
Nature communications – 12 mars 2024
DOI : 10.1038/s41467-024-45022-7
Marie Villares a effectué sa thèse au laboratoire Épigénétique et Destin Cellulaire, dans l’équipe dirigée par le Pr Jonathan Weitzman et est actuellement en post-doctorat a l’Institut de Recherche en Infectiologie de Montpellier. Marie est lauréate de la 15e édition du Prix Jeunes Talents France L’Oréal-UNESCO Pour les Femmes et la Science et a pris part au concours international francophone Ma Thèse en 180s. Découvrez la prestation de Marie Villares.
À lire aussi
Le transport subcellulaire au service de la mémoire
Une étude issue d’une collaboration internationale, coordonnée par Nicolas Panayotis, chercheur au Saints-Pères Institute for the Neurosciences (SPPIN – CNRS/Université Paris Cité) met en lumière un rôle inattendu de l’importine β1 dans le fonctionnement des synapses...
Syndrome coronaire aigu : des premiers résultats prometteurs dans la recherche contre la récidive
À la suite d’un syndrome coronaire aigu (SCA), le risque de récidive d’événement cardiovasculaire majeur (nouvel infarctus, accident coronaire ou décès) est particulièrement élevé. En cause, une inflammation résiduelle ou chronique pour laquelle il n’existe...

Consommation de conservateurs : deux études alertent sur un risque accru de cancer et de diabète de type 2
Une consommation plus élevée d’additifs alimentaires conservateurs, utilisés dans les aliments et les boissons transformés industriellement pour prolonger leur durée de conservation, a été associée à une augmentation du risque de cancer et de diabète de type 2. Ces...

Une mère sur quatre concernée par des soins irrespectueux en maternité
S’appuyant sur l’Enquête nationale périnatale de 2021, une équipe de chercheuses associant notamment l'Université Paris Cité révèle qu’un quart des mères en France seraient concernées par des soins irrespectueux en maternité, associés à un risque accru de dépression...
